

山东罗欣药业集团股份有限公司招标公告
【规 格】以����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������吉西他滨计(1) 0.2g (����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������2) 1.0g
【包 &nb����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ������sp;装】抗生素瓶装,1瓶/����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������盒、8瓶/盒、10瓶/盒
【单 位】瓶
【批准文号】0.2g 国����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������药准字H20123341 &nb����� �������Ƴ����������� �������Ƴ������������ �������Ƴ����������� �������Ƴ�������sp; 1.0g 国药准字����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������H20123340
【药品名称】
����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ������; 通 用 名:注射用盐酸吉西他滨
英 文 名����� �������Ƴ����������� �������Ƴ����������� �������Ƴ������������ �������Ƴ�������:Gemcitabine ����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������Hydrochloride for Injec����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������tion
汉语拼����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������音:Zhusheyong Yan����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������suan Jixitabin
【成 &nbs����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������p; 份】
&nbs����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������p; 本品主要成分为盐酸吉西他滨����� �������Ƴ����������� �������Ƴ������������ �������Ƴ����������� �������Ƴ�������
&����� ����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ��������������Ƴ�������nbsp;&nbs����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������p; 化学名称:(+)2′—脱氧����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������-2′,2′—二氟胞嘧啶盐酸����� �������Ƴ����������� �������Ƴ������������ �������Ƴ����������� �������Ƴ�������盐。
&nb����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������sp; 结构式:
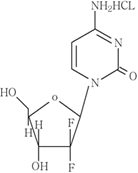
分子式:C����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������9H12ClF2N3O4
����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������� 分子量:299.66
辅&����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������nbsp; 料:甘露醇、醋酸钠。
【性 &nb����� �������Ƴ����������� �������Ƴ������������ �������Ƴ����������� �������Ƴ�������sp; 状】本品为白色疏松块状物或粉末。
【规 &����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������nbsp; 格】以吉西他滨计(����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ������1) 0.2g (2) 1.0g
【不良反应】
临床研究资料
血液和淋巴系统:
由于吉西他滨是一种骨髓抑制剂,贫血、白细胞减少����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������症和血小板减少症都有可能出现在给予吉西他����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������滨治疗之后。发热性中性粒����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������细胞减少症也常有报告。
胃肠系统:
肝功能异常非常常见,但是往往只是轻度和非进����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������展性的,因肝功能异常而导致治疗终止的情����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������况罕见。
恶心和恶心伴有呕吐非常常见。极少需要减少药物剂量����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������,并且很容易用抗呕吐药物控制����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������。
腹泻和口腔炎也经常被报告。
生殖—泌尿系统:
轻度蛋白尿和血尿非常常见
皮肤和附属器官:
皮疹非常常见,且经常与瘙痒相关。皮疹通常是轻����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������度的。脱发(通常是轻度脱发)也常有报告����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������。
呼吸系统:
呼吸困难常有报告。静脉滴注吉西他滨后发生支气管痉����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ������挛的报告不多。如果己知患者对吉西����� �������Ƴ����������� �������Ƴ������������ �������Ƴ����������� �������Ƴ�������他滨高度过敏就不应该再给予此药。
目前有关间质性肺炎的报告不多。
全身:
流感样症状非常常见。发热、头����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������痛、寒战、肌痛、乏力和厌食都是最常见的症状。
咳嗽、鼻炎、不适和出汗也常有报告。发热����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������和乏力也常常是单独出现的症状。
超敏性:严重过敏反应的报告非常罕见。
放射毒性已有报告(见【药物相互作用】)。
亦常见嗜睡的不良反应报道����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������。
心血管系统:
水肿/周围性水肿的报告非常常见。少数����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������病例报告出现了低血压。有的研����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������究报告有心肌梗塞。
上市后资料
呼吸系统:
&n����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������bsp; 与吉西他滨治疗相关的肺部症状或者严重肺����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������部症状(如肺水肿、间质性����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������肺炎或成人呼吸窘迫综合征(����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������ARDS))报告很少。这些肺部����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������症状的病因目前尚不清楚。一旦发����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������生,应考虑停用吉西他滨。早����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������期采用支持治疗措施可能有助于缓解病情。
生殖—泌尿系统:
在接受吉西他滨治疗的患者中,很少出现类似����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������溶血性尿毒症综合征(HUS)的临床表现。����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ������若有微血管性溶血性贫血的表现,如伴血小板减少����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������症的血色素迅速下降,血清胆红素水平、肌酐����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������水平、尿素氮或乳酸脱氢酶水平升高,应立即����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������停药。即使停药,患者的肾功能损伤也可能为不可逆的����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������,因此应该给予透析治疗。
心血管系统:
心衰的报告非常罕见。曾有过心律失常,特别是室上性����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������心律失常的报告。
血管:
与外周性血管炎和坏疽相关的临床表现报告非常罕见。����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������
皮肤和附属器官:
严重的皮肤反应,包括剥脱性皮炎和大疱性皮����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������疹的报告非常罕见。
有报告经连续的放射治疗和吉西他滨治疗后����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������,在以前放疗过的部位出现����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������严重的皮肤和皮肌炎类型的肌肉病征。
肝胆系统:
肝功能指标增加,包括谷草转氨酶(A����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������ST)、谷丙转氨酶(ALT����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ������)、γ-谷氨酰转肽酶(GGT)、碱性磷����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������酸酶和胆红素水平的升高的报告罕见。����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������
损伤、中毒和病程中出现的并发����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������症:
曾有过放射记忆反应的报告。
【禁 ����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������忌】
—对吉西他滨或任何辅料高度过敏的患者
—吉西他滨与放射治疗同时联合应用(由于辐射����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������敏化和发生严重肺及食道纤维样变性的危险����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������)。
—在严重肾功能不全的患者中联合应用吉西他滨与顺����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������铂。
【注意事项】
延长输液时间和增加给药频率都可能����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������增加毒性。
血液学毒性
吉西他滨可能引起骨髓功能抑制,应用����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������后可出现白细胞减少、血小板����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������减少和贫血。
患者在每次接受吉西他滨治疗前,必须监测血小板����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������、白细胞、粒细胞计数。当证实有药物引起的骨髓抑制����� �������Ƴ����������� �������Ƴ����������� �������Ƴ������������ �������Ƴ������时,应暂停化疗或修改治疗方案(见【用法����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������用量】)。然而,骨髓抑制持续时间短,通常不����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ������需降低剂量,很少有停止治疗情况发����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������生。
停用吉西他滨后,外周血细胞����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������计数可能继续下降。骨髓功能受损����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ������的患者,用药应当谨慎。与其它的抗肿����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������瘤药物配伍进行联合或序贯化疗����� �������Ƴ������������ �������Ƴ����������� �������Ƴ����������� �������Ƴ�������时,应考虑对骨髓抑制作用的蓄积。
肝功能不全
给已经出现肝转移的患者或����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������既往有肝炎、酗酒或肝硬化病史����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ������的患者使用吉西他滨,可能会导致潜在肝功能不全����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������恶化。
应定期对患者进行肾和肝功能(色括����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������病毒学检查)的实验室评价。
由于没有从临床研究中获得关于这����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������些患者群明确剂量推荐的充分信����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������息,因此,对于有肝功能不全或肾功����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������能损伤的患者,应该慎用吉����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������西他滨,因为关于这类患者的临床研究资料还����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������不够充分,尚不能据此得出明确的推荐剂量。(����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������见【用法用量】)。
同步放化疗
同步放化疗(放化疗一起应����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������用或者不同治疗间的间隔≤7天):已报告有毒����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������性反应发生(详细信息和推荐剂量����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������见【药物相互作用】)。
放疗的同时给予1000mg/m2的吉西他滨可导致严重的肺或食管病变����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������。
如果吉西他滨与放射治疗连续给予,由����� ����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ��������������Ƴ���������� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ��������于严重辐射敏化的可能性,吉西����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������他滨化疗与放射治疗的间隔至少����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������4周。如果患者情况允许可缩短����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������间隔时间。
活疫苗
不推荐接受吉西他滨治疗的患者使����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������用黄热病疫苗和其它减毒活疫苗(见【药物相互作用����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������】)。
心血管系统
由于吉西他滨可引起心脏和/或心血管病症,����� �������Ƴ����������� �������Ƴ������������ �������Ƴ����������� �������Ƴ������因此具有心血管疾患病史的����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������患者使用吉西他滨时要特别谨慎����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������。
肺
与吉西他滨治疗相关的肺部症状,有时甚至是严����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������重肺部症状(如肺水肿、间质性肺炎或成人����� �������Ƴ������������ �������Ƴ����������� �������Ƴ����������� �������Ƴ�������呼吸窘迫综合征(ARDS)有所报告。这����� �������Ƴ����������� �������Ƴ������������ �������Ƴ����������� �������Ƴ�������些症状的病因尚不清楚。一旦发生,应考虑����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������停用吉西他滨。早期采用支持治疗措施可能有助于缓解����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������病情。
肾脏
在使用吉西他滨的患者中少见有类似溶血性尿毒症综合����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������征(HUS)的临床表现(见【不良反应】)����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������。若有微血管病性溶血性贫血的表现,如伴����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ������血小板减少症的血色素迅速下����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������降,血清胆红素、肌酐、尿素氮、乳酸����� �������Ƴ������������ �������Ƴ����������� �������Ƴ����������� �������Ƴ�������脱氢酶上升,应立即停药。停药后,患者肾功����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������能损伤可能为不可逆的,应����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������给予透析治疗。
生育能力
在对生育能力进行的研究中发现,吉西他滨可引起����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������雄性小鼠精子生成过少(请����� �������Ƴ����������� �������Ƴ������������ �������Ƴ����������� �������Ƴ�������见临床前安全性数据)。因此,要����� �������Ƴ����������� �������Ƴ������������ �������Ƴ����������� �������Ƴ�������告知接受吉西他滨治疗的男性,在治疗期间和����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������治疗后6个月不要生育,而且由����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������于吉西他滨治疗可能引起不育,因此应告知男性治疗����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������前保存精子。
钠
规格为200mg/瓶的吉西他滨中����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������含有钠3.5mg(<����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������;1mmol),患者应考虑控制钠摄入����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������。
规格为1000mg/瓶的吉西他����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������滨中含有钠17.5mg(<1m����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������mol),患者应考虑控制钠摄入。
对驾驶和操纵机械的影响
尚未进行关于吉西他滨对驾驶和操纵机械影响的研究。����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������但已有报告显示吉西他滨可引起轻到中����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������度困倦,特别是在用药期间饮用酒精类饮料。因此患����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������者在此期间必须禁止驾驶和操纵机器,直到鉴����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������定已不再倦怠。
不相容性
除了[制备处置操作特别注意事项]中����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������规定的药品外,本品不得和其它药品混合。
【孕妇及哺乳期妇女用药】
妊娠
尚未有足够的数据确立吉西他滨在妊娠妇女中的安全����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������性。动物实验表明具有生殖毒性(见临床前安全性����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������数据)。根据动物实验结果和吉西他滨����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������作用机制,妊娠期妇女应避免应用吉西����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������他滨,除非有明确的必要性。应告知女性在����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ������吉西他滨治疗期间避免妊娠,一旦怀孕,应立即����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������通知其主治医生。
哺乳期
尚不明确吉西他滨是否可从乳汁分泌,其对哺乳期幼儿����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������的不良反应不能排除。在接受吉西他滨治疗期间必����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������须停止哺乳。
生育能力
在对生育能力进行的研究中发现,吉西他滨����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������可引起雄性小鼠精子生成过少(见临床前安全性数����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������据)。因此,要告知接受吉西他滨治疗的����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������男性,在治疗期间和治疗后6个月不要生育,����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ������而且,由于吉西他滨治疗可能引起不育,����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������因此应告知男性治疗前保存精子。
【儿童用药】
由于没有充分的数据支持儿童用药的����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������有效性及安全性,因此不推荐将吉西他滨用于18����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������岁以下的儿童。
【老年用药】
年龄在65岁以上的患者对吉西他滨的耐受����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ������性良好,除了对所有患者推荐的����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������剂量调整外,没有证据显示有必����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������要对老年患者进行特别的剂量调整。
【药物相互作用】
未进行特别的相互作用研究。(见【药代动力学】)
放射治疗
同步放化疗(放化疗同时应用或者不同治疗����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������间的间隔≤7天)—与这种多学科综合治疗����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������有关的毒性取决于许多不同的因素,其中包����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������括吉西他滨的剂量、吉西他滨����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������的给药频率、放射治疗的剂量����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������、放疗采用的技术、靶组织和靶体积����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������等。临床前研究和临床研究显示,吉西他滨����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������具有放疗增敏作用。在一单项����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������研究中,非小细胞肺癌患者在连续6周内同时接����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������受剂量为1,000mg/����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������m2的吉西他滨治疗和胸部治疗性放疗,观察����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������到患者出现严重的、具有潜在致命性的粘膜炎,特别是����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������食道炎和肺炎,正在接受大剂量放疗的患者尤其����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������如此[中位放疗体积(median ����� �������Ƴ����������� �������Ƴ������������ �������Ƴ����������� �������Ƴ�������treatment volum����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������es)4,795cm3]。此后进行的研究表明,在了解可预测毒性����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������的情况下,进行放疗的同时给予相对低剂量的吉西他滨����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������治疗是可行的。例如在一项非小细胞肺癌II期临����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ������床研究中,在6周的时间里同时给予了剂����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������量为66Gy的胸部放疗、吉西他滨(60����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������0mg/m2,4次)和顺铂(80mg/m2,2次)联合治疗。目前尚未在全部肿瘤类型����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������中确定用吉西他滨与放疗同时����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������应用的最佳安全治疗方案。
非同步放化疗(间隔>7天)—数据分析显����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������示,在放疗前后7天以上的时间里应用吉西����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������他滨治疗,不会使毒性增加,但可能出现放����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������射记忆反应。研究资料显示,吉西他滨治疗����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������应在放疗急性反应好转以后或者放疗结束至少1����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������周之后才能进行。
目前已有靶组织出现放射损伤的报告(����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������如食道炎、大肠炎和肺炎),这些损伤与患者放����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������疗时同时或不同时应用的吉����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������西他滨相关。
其他
由于存在引起全身性并可能是致命性疾病����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������的风险,因此,不推荐使用黄热����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������病疫苗和其它减毒活疫苗,
特别是对免疫抑制患者。
【药物过量】
尚无已知的针对吉西他滨过����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������量的解毒剂。在I期研究中有几例患者接受����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������每2周单次给予吉西他滨静脉滴注570����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������0mg/m2,输注时间30分钟以上,观����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������察的主要毒����� ���������� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ���������Ƴ�������性包括骨髓抑制、感觉异常和严����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ������重皮疹等。临床一旦怀疑有过量情况,应����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������对血液学指标进行适当的监测,����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������必要时对患者进行支持治疗。
【药理毒理】
药理作用
作用机制:
细胞代谢和作用机制:吉西他滨����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������(dFdC)为嘧啶类抗代谢物,在细胞内����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������经核苷激酶的作用被代谢为具有活����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������性的二磷酸( dFdCDP)及三磷酸����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������核苷(dFdCTP)。dF����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������dCDP和dFdCTP通过两种作用机����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������制抑制DNA合成,从而实现吉西他滨的细胞毒作����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������用。首先,dFdCDP抑制核苷酸还����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������原酶的活性,致使合成DNA所必需的三磷酸脱氧����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������核苷(dCTP)的生成受到抑制。其次,dF����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������dCTP与dCTP竞争掺����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������入至DNA链中(自增强作用)。同样,少量的����� �������Ƴ����������� �������Ƴ����������� �������Ƴ������������ �������Ƴ�������吉西他滨还可以掺入RNA分子中。因此,细胞内dC����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������TP浓度降低更加有利于dF����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������dCTP掺入到DNA链中。DNA聚合酶����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������ε不能去除掺入的吉西他滨及修复已形成的DNA����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������链。吉西他滨掺入DNA链后����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������,延伸的DNA链中就增加����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������了一个核苷酸。这个增加的核苷酸可以完����� �������Ƴ������������ �������Ƴ����������� �������Ƴ����������� �������Ƴ�������全抑制DNA链的进一步合成(隐蔽链终止)。吉西他����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������滨掺入DNA链后引起细胞凋亡。����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������
对培养细胞的细胞毒活性:
吉西他滨对各种培养的人及鼠肿瘤细胞有明显的细胞����� �������Ƴ����������� �������Ƴ������������ �������Ƴ����������� �������Ƴ�������毒活性。其作用具有细胞周期����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������特异性,即吉西他滨主要作用于DN����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������A合成期(S一期)的细胞,在一定的条件����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������下,可以阻止Gl期/S期交接点的细胞进����� �������Ƴ����������� �������Ƴ����������� �������Ƴ����������� �������Ƴ�������展。在体外,吉西他滨的细胞毒作用取决于浓度和����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������时间。
动物模型中抗瘤活性的研究:
在肿瘤动物模型的研究中发����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������现吉西他滨的抗肿瘤活性与给药的����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������方式有关。每天给药的方法会导����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������致动物死亡率很高,而抗肿瘤活����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������性很低。当用每3~4天给药����� �������Ƴ������������ �������Ƴ����������� �������Ƴ����������� �������Ƴ�������一次的方法,吉西他滨在非致死剂量时对小鼠的����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������多种肿瘤均有很好的抗肿瘤活性。
毒理作用
在鼠及犬为期6个月的重复剂量����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������研究中,主要发现有可逆的剂量依赖����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������性的造血功能的抑制。
遗传毒性
在体外突变实验和体内骨髓微核试验中发现,吉����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������西他滨可致突变。尚未进行评����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������价致癌可能性的长期动物研究。
在生育能力研究中发现,吉西他滨可以引起雄性小鼠可����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������逆性精子发生过少。尚未发����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������现对雌性动物的生育能力有影响。
动物试验表明吉西他滨具有生殖毒性,如导致新生动物����� �������Ƴ����������� �������Ƴ������������ �������Ƴ����������� �������Ƴ�������的生理缺陷或对胚胎或胎儿发育、妊娠过����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������程或围产期及产后期的其他影响等。
【药代动力学】
药代动力学特点
在7项研究,共计353例患者中����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������评价了吉西他滨的药代动力学����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������特点。其中女性患者121例和男性患者232����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������例,年龄29~79岁之间。在这����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������些患者中,约45%为非小细胞肺癌患者,35%����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������为胰腺癌患者。得到以下药����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������代动力学参数的给药剂量范围是500~2,5����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������92mg/m2,输液时间变化范围0.4~1.2小时。&����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������nbsp; ����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������;
血浆峰浓度(输液结束后5分钟内得到)为����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������3.2~45.5μg/ml����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������。按照1000mg/m2/30min����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������剂量给药,输液结束30min内母体化合����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������物血浆浓度可持续高于5μg/ml,输液结束����� �������Ƴ������������ �������Ƴ����������� �������Ƴ����������� �������Ƴ�������后1小时内,其血浆浓度亦高于0.4μg/ml����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������。
分布
中央室的分布容积为女性12.4 L/m2和男性����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������17.5L/m2(个体间差异为91.9%)。周边隔室的分布����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������容积为47.4 L/m2。周边隔室的容积与性别不相关����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������。
血浆蛋白结合可忽略不计。 ����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ������� ����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������
半衰期:半衰期为42~94分钟,与年龄和性别����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������相关。对于推荐的给药方案,吉西他滨在输液开始后的����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������5~11小时内被完全清除。每周给药一次����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������时,吉西他滨不会产生蓄积。
代谢
吉西他滨在肝脏、肾脏、血液和其它组织中被����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������胞苷脱氨酶快速代谢。在细胞内����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������,吉西他滨在细胞内代谢产生吉西����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������他滨单磷酸、二磷酸和三磷����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������酸核苷(dFdCMP、dFdCDP和dFdC����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������TP),其中dFdCDP和d����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ������FdCTP具有活性。这些细胞内����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������形成的代谢物,在血浆或尿液中����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������都未曾检出。主要代谢物2’—脱����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������氧—2’,2’—二氟尿苷(dFd����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������U)没有活性,在血浆和尿中均可检出����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������。
排泄
全身清除率为29.2 L/hr/m2~92.2L/hr/m2,与性别和年龄相关(个体差异为52.2%)。清除����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������率女性比男性低大约25%。虽然清除速度很快,男性����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������和女性的清除率都随年龄增加而下降。吉西����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������他滨推荐给药剂量为1000m����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������g/m2,静脉滴注30分钟,不必因男性和����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������女性降低的清除率而减少吉西他滨的给药剂量����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������。
经尿排泄:少于10%以原药形式排泄����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������。
肾清除:2~7L/hr/m2。
给药后一周内,吉西他滨给药����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������剂量的92~98%被检出����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������,其中99%主要以dFdU形式经尿����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������排泄,1%经粪便排泄。
dFdCTP的动力学
这一代谢物发现于外周血的单����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������核细胞中,以下信息均指在这类细����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������胞中的情况。按35~350mg/����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������m2/30min给药,dFdCTP在细胞内����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������浓度的递增与剂量增加成比例,药物����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������的稳态浓度为0.4~5μg/ml。吉西他滨血����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������浆浓度超过5μg/ml时,dFdCTP浓度不����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������再增����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������加,表明已在细胞内饱和。
终末消除半衰期:0.7~12小时。
dFdU的动力学特点
血浆峰浓度(1000mg/m2,静脉滴注3����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������0分钟,结束后3~15分钟):2����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������8~52μg/ml。
每周一次给药后谷浓度:0.07����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������~1.12μg/ml,无明显蓄积。
三相药时曲线终末期平均半衰期-65����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������小时(范围33~84小时)。
dFdU从母体药物中形成的比����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������例:91%~98%。
中央室平均分布容积:18L����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������/m2(范围11~22L/����� �������Ƴ����������� �������Ƴ������������ �������Ƴ����������� �������Ƴ�������m2)。
平均稳态分布容积(Vss):150L/����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������m2(范围96~228L/m2)。
组织分布:广泛。
平均表观清除率:2.5L/hr/����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������m2(范围1~4L/hr/m2)。
经尿排泄:全部。 ����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������;
吉西他滨与紫杉醇联合治疗
联合治疗并不改变吉西他滨或紫����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ������杉醇的药代动力学特点。
肾功能损伤
轻到中度的肾功能不全(GFR从30ml/mi����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������n~80ml/min),对吉西他滨药代动力学特����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������点并没有出现一致性的显著影响。����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������
【贮 藏】遮����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������光、密闭,在干燥处保存。
【包 ����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������; 装】抗生素瓶装,1瓶/盒����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������、8瓶/盒、10瓶/盒
【有 效 期】24个月
【执行标准】《中国药典》2015年版二部
【批准文号】0.2g 国药����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������准字H20123341 ����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������1.0g 国药准字H201233����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������40
【生产企业】
&nb����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������sp; 企业名称:山东罗欣药业集团股份有限公����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������司
&n����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������bsp; 生产地址:山东省临����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������沂高新技术产业开发区罗七路
����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������邮政编码:276017
电话号����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������码:0539-8257899 84����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������81991
传真号码:����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������0539-8481990
����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������� 售后服务:0539-82426����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������99
网&����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������nbsp; &n����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������bsp; 址:www.luoxin.cn
本品可用于治疗以下疾病:
—局部晚期或己转����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������移的非小细胞肺癌;
—局部晚期����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������或已转移的胰腺癌;
—吉西他滨与紫杉醇联����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������合,可用于治疗经辅助/新����� �������Ƴ����������� �������Ƴ����������� �������Ƴ������������ �������Ƴ�������辅助化疗后复发,不能切除的、局部复����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������发或转移性乳腺癌。除非临床上有禁忌,否����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������则既往化疗中应使用过蒽环类抗生素。
本品应在有经验的肿瘤学专家指导下使����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������用。建议参考已有临床试验����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������资料根据临床个体情况调节用量。
剂量
成人:
非小细胞肺癌
单药治疗:
吉西他滨的推荐剂量为1000mg/m2,静脉滴注30分钟。每周给药1次����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������,治疗3周后休息1周。重复上述的4周治疗周期����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������。根据患者对吉西他滨的耐受性可考虑在每个治疗����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������周期或一个治疗周期内降低剂量。
联合治疗:
吉西他滨与顺铂联合治疗有两����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������种治疗方案:3周疗法和4����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������周疗法。
3周疗法:吉西他滨的推荐剂量为125����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������0mg/m2,静脉滴注30分钟。每21天治疗周期的第1天和����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������第8天给药。根据患者对吉西他滨的耐受性可考虑在每����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������个治疗周期或一个治疗周期内降����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������低剂量。
4周疗法:吉西他滨的推荐����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������剂量为1000mg/m2,静脉滴注30分钟。每28天����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������治疗周期的第1天、第8天和第����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������15天给药。根据患者对吉西他滨的耐����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������受性可考虑在每个治疗周期或一����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������个治疗周期内降低剂量。
胰腺癌
吉西他滨推荐剂量为1000mg/m2,静脉滴注30分钟。每周1次,连续7周����� �������Ƴ����������� �������Ƴ����������� �������Ƴ������������ �������Ƴ�������,随后休息1周。随后的治疗����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������周期改为4周疗法:每周1次给药,连续治����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������疗3周,随后休息1周。根����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������据患者对吉西他滨的耐受性可考虑在每个治疗周����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������期或一个治疗周期内降低剂量。
乳腺癌
推荐吉西他滨与紫杉醇联合给药。在每21天治疗周期����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������的第1天给予紫杉醇(175mg/m2),静脉滴注约3小时,随后����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������在第1天和第8天给予吉西他����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������滨(1250mg/m2),静脉滴注30分钟。根据患者对吉西他滨����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������的耐受性可考虑在每个治疗����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������周期或一个治疗周期内降低剂量。在����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������接受吉西他滨十紫杉醇联合化疗之����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������前,患者的粒细胞绝对计数应至少为1,500 ����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������(×106/L)。
毒性监测和根据毒性进行的剂量调整
因非血液毒性进行的剂量调整
使用吉西他滨的患者应定期����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������进行肝、肾功能的临床常规检查,以检测是否发生����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������非血液学毒性。根据患者对吉西他滨的耐受性可考虑在����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������每个治疗周期或一个治疗周期内降低剂量。通����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������常,对于除恶心/呕吐外的����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������严重(3或4级)的非血液学毒性,����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������应停止吉西他滨治疗或由医生判断减����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������量治疗。根据临床医生的意见可考����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������虑停止治疗直至毒性反应消失。
对于顺铂、卡铂和紫杉醇在联合给药时的剂量调整����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������,请参照相关产品的����� ������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������������Ƴ�������说明书。����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������
因血液学毒性进行的剂量调整
治疗周期开始
对于所有适应症,每次使用吉西他滨前,����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������必须对患者进行血小板和粒细胞计数检查。在每个����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������治疗周期开始前,患者的粒����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������细胞绝对计数应不少于1,5����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������00(×106/L),且血小板计数需达����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������到100,000(×106/L)。
治疗周期内
治疗周期内吉西他滨的剂量调整应该根据下面����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������的表格进行:
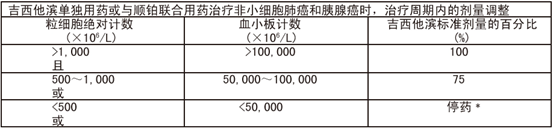
﹡在该治疗周期内,在粒细胞绝对计数未恢复到����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������至少500(×106/L),血小板计数未恢复到至少50,000(×1����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������06/L)时,不能恢复治疗。����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ������
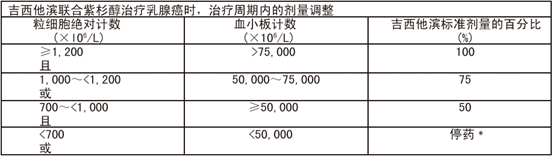
﹡在治疗周期内不能恢复治疗。下一����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������周期的第1天,若患者粒细胞����� �������Ƴ����������� �������Ƴ������������ �������Ƴ����������� �������Ƴ�������绝对计数达到至少1,50����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������0(×106/L),血小板计数达到100,000(×106/L),可开始治疗。
对于所有适应症,按血液学毒性对相继的下����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������一治疗周期进行的剂量调整
出现下列血液学毒性时,吉西他滨的剂量应当减����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������少至最初治疗周期使用剂量的75%。
•粒细胞绝对计数<����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������500×106/L持续5天以上
•粒细胞绝对计数<10����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������0×106/L持续3天以上
•发热性中性粒细胞减少症����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������
•血小板<����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������25,000×106/L
•由于毒性治疗周期延迟一周以上����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������。
给药方法
吉西他滨在输液期间耐受性很好,给药方便。如����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������果发生外渗,应立即停止输液����� �������Ƴ����������� �������Ƴ����������� �������Ƴ����������� �������Ƴ�������,更换血管重新开始输液。����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������给药后应对患者进行密切观察。若发生非静����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������脉途径给药,必须立即停止给药。
制备、处置和其它操作特别注意事����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ������项
操作
制备和处置输液时,必须阅读细胞抑制剂的常����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������规操作安全注意事项。应在安全箱中处理输液,穿着防����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������护服和佩戴防护手套。如果没有安全箱还����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������应佩戴防护面罩和防护眼镜。
如果所制备溶液与眼睛接触,����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������可能引起严重的刺激,应立即用水彻底����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������冲洗眼睛。
如果持续刺激,应咨询医生。如果溶液����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������溅到皮肤上,应用水彻底冲洗。
重新溶解(和进一步稀释,����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������如适用)操作指导
浓度为9mg/ml(0.9%)的����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������氯化钠注射液(不含防腐剂)是唯一被允许用于重新溶����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������解吉西他滨无菌粉末的溶液。根据药物的溶����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������解性,重新溶解后吉西他滨浓度不应超过40m����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������g/ml。如果重新溶解溶液浓度大于40����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������mg/ml,可能会导致药物溶解����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������不完全,应该避免。
1.重新溶解及进一步稀释静脉滴注用����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������吉西他滨时应无菌操作。
2.重新溶解时,将5ml浓����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������度为9mg/ml(0.9%)的无菌����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������无防腐剂的氯化钠注射液加入到200mg规格的����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������小瓶中或将25ml浓度为9mg/����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������ml(0.9%)的无菌无防腐剂的����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������氯化钠注射液加入到1000mg规格的小����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������瓶中。重新溶解后溶液的总����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������体积分别是5.26ml(200mg规格)或2����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������6.3ml(1000mg规����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������格)。溶解后得到吉西他滨的浓度是38mg/����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������ml,计算时包括了冻干粉的����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������排水体积。震摇至溶解。可以用9mg/����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������ml (0.9%)无菌无防腐剂的氯化����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������钠注射液进一步稀释。重新溶解的溶液是澄清����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������无色至淡黄色的液体。
3.注射用药品溶液在使用前需����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������检查是否存在不溶性颗粒物和����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������是否褪色。如果发现有颗粒物,则不能使用。����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������
任何未使用过的产品或废弃物都应根据当地要求处置����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������。
特殊人群
肾或肝损伤患者
对于肝或肾功能不全的患者,应当慎用吉����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������西他滨,因为关于这类患者的临床研究资料还不够����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������充分,尚不能据此得出明确的推荐剂����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ������量(见【注意事项】和【药代动力����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������学】)。