

山东罗欣药业集团股份有限公司招标公����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������告
近日,罗欣药业(002793.SZ)下属子公司山����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������东罗欣药业集团股份有限公����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ������司、罗欣药业(上海)有限公����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������司收到国家药品监督管理局下发的注射用LX����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������22001的《药物临床试验批准通知书》。注射用LX22001是罗欣药����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������业创新药替戈拉生的注射剂型,是钾离子竞争性����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������酸阻滞剂类药物(P-CAB),����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������目前在全球范围内尚无产品上市。
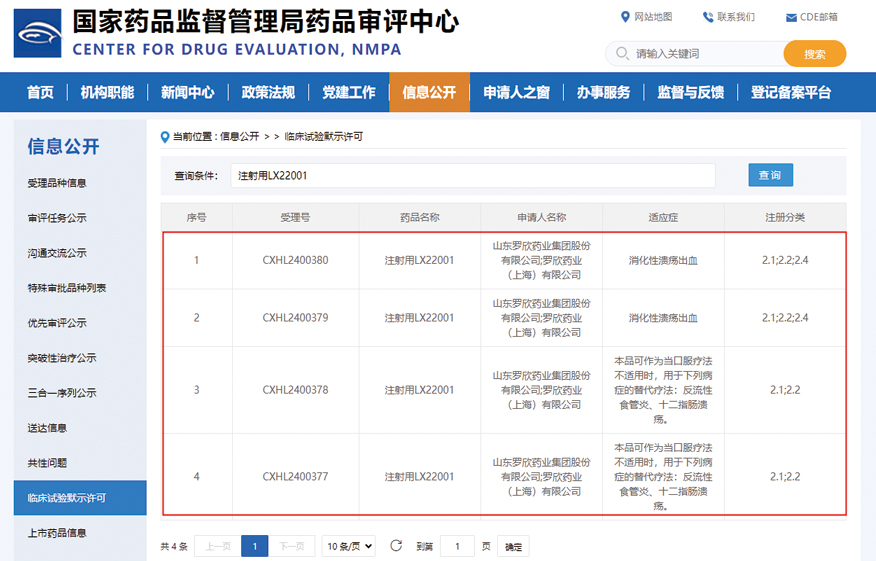
图为:国家药品监督管理局药品审评中心公示
此次获准临床的注射用LX22001开发适应����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������症为:(1)本品可作为当口服疗����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������法不适用时,用于下列病症的替代疗����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������法:反流性食管炎、十二指肠溃疡;(2)消化性溃疡����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������出血。
作为全新机制的P-CAB相比于����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������传统质子泵抑制剂(PPI),具有更快速起效、更强效持久抑酸����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������、服用更方便等特点,首剂即可达到更大抑酸效果����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������,有效抑制夜间酸突破等优势[1][2]。目前,最新的中国消化领域疾病����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������指南已将P-CAB口服剂型作为反流性食管����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ������炎的首选药物之一[3]。注射剂型的临床应用场景����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������与口服剂型存在差异,更多应用于手术、����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������住院等。随着P-CAB被越来越多的����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������专家、患者认可,未来有望成为主流抑酸����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������药物逐渐替代PPIs。
近年来,罗欣药业加速创新����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������转型,坚持“自主研发+合作研发”双轨并进,聚����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������焦优势领域,逐步打造了以消化、呼吸系统疾病为����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������主线、兼顾抗肿瘤等治疗领域的创新产品����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������研发管线,多个创新产品为临床用药带����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������来新选择。
2022年4月,公司首款1类����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������新药替戈拉生片“反流性食管炎”适应症获����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������批上市,已被纳入《国家基本医疗保险、����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ������工伤保险和生育保险药品目录����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������(2022年)》。
2023年11月,替戈拉生片新����� �������Ƴ����������� �������Ƴ����������� �������Ƴ������������ �������Ƴ�������增“十二指肠溃疡”适应症获批����� �������Ƴ����������� �������Ƴ������������ �������Ƴ����������� �������Ƴ�������上市。
2023年12月,替戈拉生片����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������新适应症“与适当的抗菌疗法联用根除幽门螺杆菌����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������”上市申请获得国家药品监督管理局受理,该����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������适应症的临床数据根除率优效于对照组艾司����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������奥美拉唑,为该适应症首个根除率超90%的P-C����� �������Ƴ����������� �������Ƴ����������� �������Ƴ����������� �������Ƴ�������AB。
2024年5月,替戈拉生片新适应症“与适当����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������的抗菌疗法联用根除幽门螺杆菌”III期����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ������临床研究入选2024年美国消化疾病周(����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������DDW)口头报告[4]。
2024年1月,公司消化领域布局的另一款����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ������新药普卡那肽片的Ⅲ期临床试验已完成,达����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������成主要疗效终点,有望成为国内首个治疗慢性特发性����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������便秘的鸟苷酸环化酶激动剂。
2024年6月,罗欣药业与����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������国际领先的AI+BT微生����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������态研发企业深圳未知君就肠道菌群移植技术(FMT)����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������在合作区域内合作范围的独家代理经销合作达成����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������一致意见。
深耕医药行业36年,罗欣药业将持续秉持����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������“传递健康”理念,深入实施科技创新,关注未����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������被满足的临床需求,持续推进高质量创新药品研发成����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������果落地,为全球患者提供更多创新药����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������物选择。
参考文献:
[1].Hunt RH, et al. ����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������Curr Treat Options����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ������� Gastroenterol.2018 Dec;����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ������16(4):570-590.
[2].Kim JS, Seo ����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������SI, Kang SH, Lee SK����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������, Kim AR, Park HW,����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������� Kim BT, Song GS. Ef����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������fects of Tegoprazan V����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ�������ersus Esomeprazo����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������le on Nighttime Hea����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������rtburn and Sle����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������ep Quality in Gast����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������roesophageal Reflux D����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������isease: A Multicenter Do����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������uble-blind Randomized����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ������� Controlled Trial. J����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������� Neurogastroenter����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������ol Motil. 2023 Ja����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������n 30;29(1):5����� �������Ƴ����������� �������Ƴ������������ �������Ƴ������������ �������Ƴ�������8-64.
[3]. 中华医学会消化病学分会.2020����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������年中国胃食管反流病专家共识[J����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������].中华消化杂志, 2020,����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������� 40(10):649-663.
[4].Liya Zhou����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������, Zhiqiang Song. A����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ������� MULTICENTER,����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ������� RANDOMIZED, DOUBLE-BL����� �������Ƴ������������ �������Ƴ������������ �������Ƴ����������� �������Ƴ�������IND, DOUBLE-DUMMY����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ������� PHASE III CLINICAL STU����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������DY EVALUATING����� �������Ƴ������������ �������Ƴ����������� �������Ƴ������������ �������Ƴ������� THE EFFICACY AND S����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������AFETY OF BISMUTH ����� �������Ƴ����������� �������Ƴ����������� �������Ƴ������������ �������Ƴ�������QUADRUPLE THERAPY CO����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������NTAINING TEGOPRAZAN ����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������COMPARED TO ESOMEPRAZ����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������OLE IN ERADI����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������CATING HELICOBACTER PY����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������LORI IN CHINA. ����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������Presentation Numbe����� �������Ƴ������������ �������Ƴ������������ �������Ƴ������������ �������Ƴ�������r: 6562.